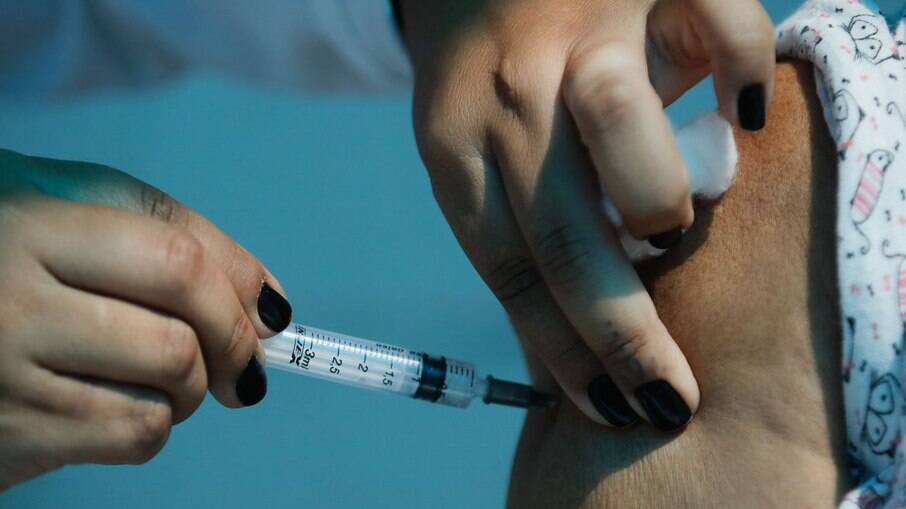
A Agência Europeia de Medicamentos (EMA, termo em inglês) anunciou, nesta terça-feira (4), que deu início a uma revisão contínua
da CoronaVac, vacina contra a Covid-19. De acordo com o órgão, esse é o primeiro passo para um pedido de autorização formal de comercialização na União Europeia.
Por meio de nota, a agência explicou que vai avaliar os dados para decidir se os benefícios da vacina superam os riscos. Até o momento, a CoronaVac já foi autorizada para uso no Brasil, China, Indonésia e Turquia.
"Esses estudos sugerem que a vacina desencadeia a produção de anticorpos que têm como alvo o Sars-CoV-2, o vírus que causa a Covid-19, e pode ajudar a proteger contra a doença", diz o texto. A revisão contínua é uma ferramenta da EMA para acelerar a avalição de um medicamento durante uma emergência de saúde pública.
Outras três vacinas estão sendo submetidas a uma análise contínua pela agência: CureVac, Novavax e Sputnik V. Já foram incluídas na lista da OMS as vacinas da Pfizer, Moderna, Oxford/AstraZeneca e Johnson (as mesmas aprovadas pela União Europeia).
