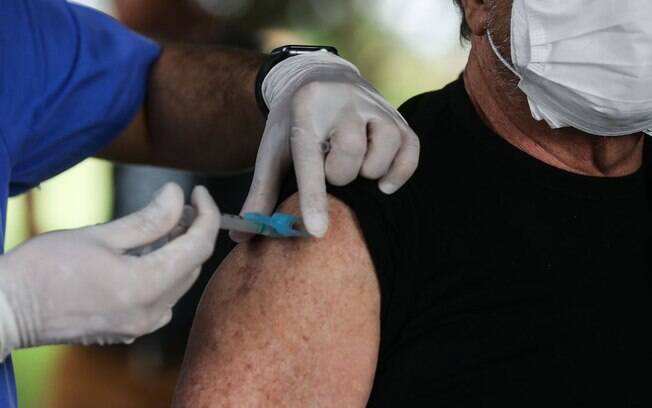
A farmacêutica americana Pfizer anunciou nesta quarta-feira (18) que sua vacina candidata contra a Covid-19 é 95% eficaz e que solicitará à Food and Drug Administration (FDA), agencia americana equivalente à Anvisa no Brasil, o uso emergencial do imunizante. Na semana passada, a companhia divulgou resultados preliminares que apontavam para a segurança da fórmula e uma eficácia acima de 90%.
A Pfizer informou, ainda, que 170 voluntários contraíram a Covid-19, dos quais apenas oito haviam sido imunizados. Os demais 162 estavam no grupo placebo — ou seja, que não recebeu a vacina. Dez pessoas apresentaram sintomas graves de Covid-19, mas apenas uma delas foi imunizada.
A farmacêutica informou que o imunizante também se mostrou efetivo em diferentes faixas etárias e grupos étnicos e demográficos. A eficácia em idosos acima de 65 anos, que compõem um dos principais grupos de risco da Covid-19, foi de 94%. Nenhum efeito colateral significativo foi reportado entre os 43 mil voluntários, uma indicação, na avaliação da empresa, que a vacina pode ser implementada de forma ampla ao redor do mundo.
O efeito adverso mais observado nos ensaios clínicos foi a fadiga, reportada em 3,7% dos voluntários imunizados depois da segunda dose. Adultos idosos se mostraram mais propensos a desenvolver febre e outros reflexos menores.
A farmacêutica reiterou que espera produzir até 50 milhões de doses de vacinas este ano, o suficiente para proteger 25 milhões de pessoas, e então produzir até 1,3 bilhão de doses em 2021.
Nesta semana, a concorrente americana Moderna também anunciou números promissores ao final dos ensaios clínicos. O desempenho dos dois imunizantes, baseados na inédita tecnologia de RNA mensageiro (mRNA), aumentou as expectativas por um freio à pandemia do novo coronavírus, que já matou mais de 1,3 milhão de pessoas no mundo e derrubou a economia global.
