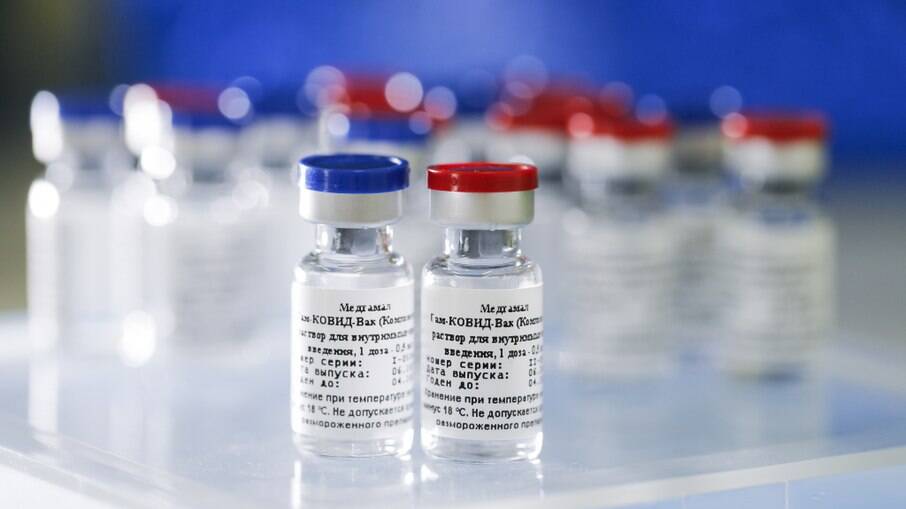
O Fundo Russo de Investimento Direto disse que vai enviar "em breve" à Agência Nacional de Vigilância Sanitária (Anvisa) o pedido de uso emergencial da Sputnik V no Brasil.
Em nota, o fundo russo disse que solicitações de informações de dados adicionais por parte dos reguladores são um procedimento padrão e "não significam que uma oferta de registro foi rejeitada".
Neste sábado (16), a Anvisa anunciou que devolveu a documentação referente ao pedido de uso emergencial ao laboratório União Química. O grupo farmacêutico foi quem protocolou em conjunto com o fundo russo a solicitação. A autorização era para que fossem liberadas 10 milhões de doses da vacina russa.
A agência informou, em nota, que a devolução aconteceu porque a documentação não apresenta "requisitos mínimos para submissão e análise."
"O pedido foi restituído à empresa por não atender os critérios mínimos, especialmente pela falta de autorização para a condução dos ensaios clínicos fase 3, a condução em andamento no país e questões relativas às boas práticas de fabricação", disse a Anvisa.
Ainda de acordo com a agência, "não basta o pedido de autorização de estudo clínico de fase 3 estar protocolado para pedir uso emergencial", pois "é necessário que tais estudos estejam em andamento no país, além de outras medidas condicionantes já previstas."
