![]()
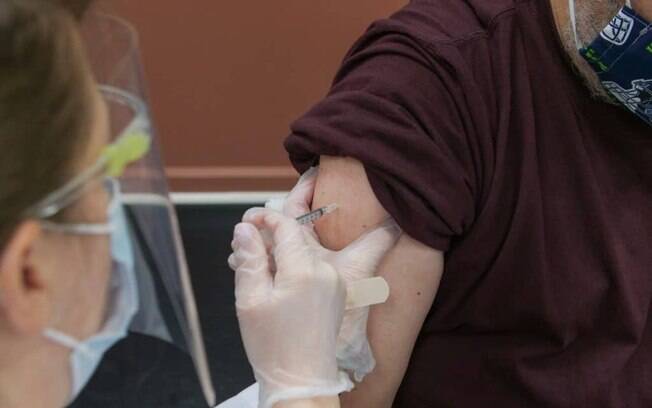
Passado pouco mais de um mês desde o início da vacinação contra a Covid-19 no Brasil, o balanço feito pela Agência Nacional de Vigilância Sanitária ( Anvisa ) sobre os eventos adversos das vacinas em uso no país é positivo. Segundo o órgão, as reações observadas não são graves e estão dentro do esperado.
A agência avalia “qualquer ocorrência médica indesejada que aconteça após a vacinação e que, não necessariamente, tenha relação causal com o uso de uma vacina ou outro imunobiológico”.
Segundo Suzie Gomes, gerente-geral de Monitoramento de Produtos Sujeitos a Vigilância Sanitária da Anvisa, os efeitos adversos da CoronaVac e da Covishield têm sido monitorados desde “a primeira agulhada”.
Ela ressalta que ainda é cedo para qualquer tipo de avaliação, mas que não houve notificação capaz de alterar o perfil de segurança dos imunizantes. “Não existe, até o momento, nenhum sinal importante para que se desencadeie um processo regulatório ou uma ação regulatória”, afirma Susie.
Segundo ela, dor de cabeça, febre e sensação de gripe foram eventos adversos mais frequentes. No entanto, nenhuma dessas reações é grave e todas são “esperadas”. Nos próximos dias, a Anvisa deve receber relatórios de benefício-risco das fabricantes Sinovac (CoronaVac) e AstraZeneca (Covishield) com dados referentes ao primeiro mês de vacinação no país . Essas informações reforçarão o monitoramento da segurança das vacinas.
Você viu?
Vacina da Pfizer
A notificação de não ocorrência de casos adversos dos imunizantes em uso no Brasil sai um dia após a Pfizer rejeitar as exigências do ministério da Saúde brasileiro para que o imunizante seja comprado pelo país. Uma das polêmicas é o fato de o governo federal não concordar em se responsabilizar se a vacina da farmacêutica apresentar efeitos adversos nos vacinados.
Esse foi um dos motivos para a substância ainda não ter sido comprada — e, nesta terça-feira (23), a fórmula foi a primeira a receber o registro definitivo da Anvisa para uso no Brasil. Outros impasses envolvem o pedido para que conflitos sejam resolvidos em uma Corte Arbitral de Nova York e condições impostas como garantia do pagamento dos imunizantes.
Via: Agência Brasil
