
A Anvisa ( Agência Nacional de Vigilância Sanitária ) anunciou nesta terça-feira (8) a suspensão imediata da comercialização, distribuição e uso do soro Ringer com Lactato fabricado pela empresa Halex Istar Indústria Farmacêutica.
A decisão foi motivada pela identificação de um desvio de qualidade no produto, após a constatação da presença de um corpo estranho em frascos do lote. A medida foi publicada no Diário Oficial da União e tem aplicação imediata em todo o território nacional.
O soro Ringer com Lactato é amplamente utilizado em procedimentos clínicos e hospitalares, principalmente em casos de reidratação e reposição de eletrólitos, como sódio, cloreto, potássio e cálcio.
Também é indicado para o tratamento e prevenção de acidose metabólica. A composição do produto inclui cloreto de sódio, cloreto de cálcio, cloreto de potássio e lactato de sódio, diluídos em água esterilizada.
Segundo a Anvisa, a presença de corpo estranho contraria diretrizes estabelecidas pela Resolução da Diretoria Colegiada, que determina que medicamentos devem ser produzidos com garantia de qualidade e segurança.
A agência ressaltou que a medida visa proteger a saúde da população e que o uso do soro está proibido até que as falhas sejam sanadas. A Halex Istar será responsável pelo recolhimento de todos os lotes afetados.
Crise no Peru
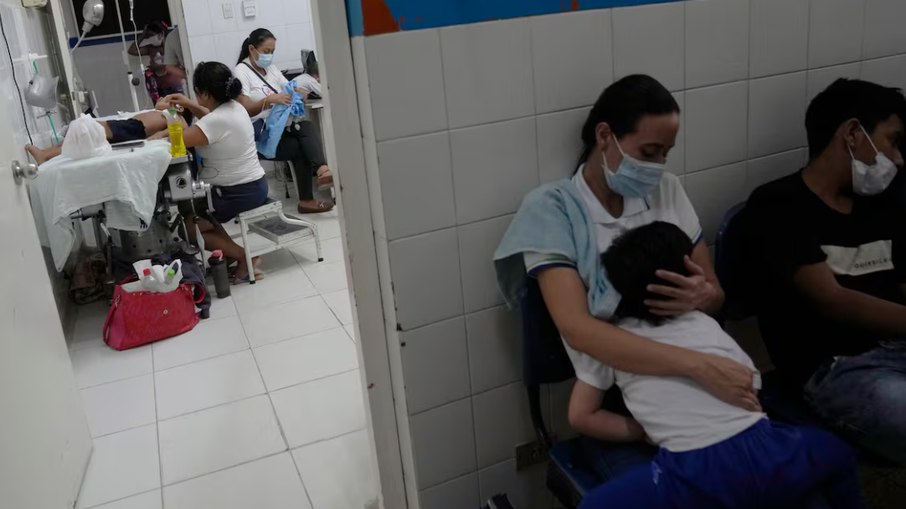
A suspensão ocorre em meio a uma crise semelhante no Peru, onde a administração de soro fisiológico contaminado provocou a morte de quatro pessoas e deixou outras 13 em estado grave.
O produto, fabricado pela empresa Medifarma, apresentava concentração de sódio muito acima do permitido, atingindo níveis potencialmente letais.
Entre as vítimas está uma criança de um ano e uma mulher de 46 anos, que receberam o soro em uma clínica particular de Lima. Em Cusco, uma jovem de 24 anos também morreu após utilizar o mesmo produto durante um procedimento estético.
Laudos indicaram que uma das vítimas chegou a apresentar 200 mEq/L de sódio no sangue, ultrapassando o limite considerado tolerável, de 165 mEq/L. Exposições a essa concentração podem causar danos neurológicos graves e levar à morte.
O laboratório Medifarma assumiu publicamente a responsabilidade, alegando falhas nos processos de produção e controle de qualidade. A empresa pediu desculpas às famílias das vítimas.
O Ministério da Saúde do Peru denunciou a companhia por crimes contra a saúde pública, mas também enfrenta críticas por ter demorado a emitir alertas sanitários.
A primeira morte foi registrada em fevereiro, mas o alerta só foi divulgado quase um mês depois. Inicialmente, acreditava-se que o lote defeituoso contava com 10 mil frascos, mas a investigação revelou o dobro: 20 mil unidades foram distribuídas, muitas delas sem rastreabilidade. Até o momento, cerca de 4 mil frascos seguem sem localização confirmada.
A crise expôs fragilidades na estrutura da Direção Geral de Medicamentos, Insumos e Drogas, órgão responsável pela fiscalização de medicamentos no Peru.
A instituição foi alvo de críticas por utilizar sistemas manuais e ter baixa autonomia técnica. O então diretor da Digemid foi exonerado e substituído, mas a nova nomeação também gerou questionamentos por supostos conflitos de interesse.
Para evitar o desabastecimento de soro nas unidades de saúde, o governo peruano adquiriu 120 mil frascos de outro fornecedor e articula a chegada de doações internacionais. Mesmo com a pressão popular, o ministro da Saúde, César Vásquez, descartou renunciar ao cargo.
Outro lado
Em nota enviada ao Portal iG, a Halex Istar Indústria Farmacêutica S.A. afirmou que o recolhimento do lote mencionado foi uma ação voluntária da própria empresa, comunicada à Anvisa em 13 de fevereiro de 2025.
A empresa ressaltou que o produto é indicado para reidratação e equilíbrio hidroeletrolítico, com uso restrito a ambientes hospitalares e sob monitoramento de profissionais de saúde.
A Halex Istar explicou que o soro é envasado em embalagem plástica frágil e que a bula recomenda inspeção visual do conteúdo antes da administração.
Segundo a nota, a composição nutritiva do soro pode favorecer o aparecimento de corpo estranho, como leveduras, em caso de rompimento da embalagem.
A farmacêutica afirmou ainda que adota medidas preventivas antes mesmo da conclusão de análises internas, e que o recolhimento de lotes eventualmente comprometidos segue o princípio da precaução.
Por fim, a empresa criticou a forma como a informação foi divulgada, afirmando que a notícia "peca pela imprecisão" ao não esclarecer que a medida da Anvisa refere-se apenas ao lote específico.
Confira a nota na íntegra abaixo:
" A HALEX ISTAR INDÚSTRIA FARMACÊUTICA S.A., havendo tomado conhecimento da matéria publicada a respeito do produto RINGER COM LACTATO¹, vem, respeitosamente, à presença de V. Sa., informar o quanto segue:
1. O produto RINGER COM LACTATO® é indicado para reidratação e restabelecimento do equilíbrio hidroeletrolítico do organismo, quando há perda de líquidos e de íons cloreto, sódio, potássio e cálcio, e para profilaxia e tratamento de acidose metabólica. O produto encontra-se regularmente registrado perante a Anvisa², e seu uso é restrito a ambientes hospitalares e ambulatoriais, o que significa que sua administração é necessariamente monitorada por profissionais de saúde.
2. Envasado em embalagem plástica e frágil, o produto exige delicadeza e cuidados imprescindíveis de armazenamento para manutenção de sua integridade, tanto que a bula³ expressamente informa ser mandatório promover a avaliação visual do aspecto do medicamento antes de ser ministrado ao paciente. E tais cuidados são relevantes porque o produto é composto de uma solução especialmente nutritiva, que pode levar à evolução de corpo estranho (leveduras), se a integridade da embalagem for comprometida e o produto tiver contato com o ambiente externo.
3. As etapas de armazenamento e transporte são imprescindíveis para manutenção da qualidade do sistema de fechamento das embalagens primárias (que é plástica), e requer cuidados especiais conforme estabelece a rotulagem, a caixa de transporte e a bula do medicamento.
4. Caso não sejam observados os cuidados de armazenagem e manuseio, o produto pode ficar sujeito a alterações de aspecto, por eventual avaria na embalagem primária, com o que se alterariam as características intrínsecas do produto. Bem por isso, é necessário, repita-se, que o medicamento seja inspecionado visualmente pelo profissional da saúde, antes do produto ser administrado ao paciente, mitigando eventuais riscos à saúde.
5. E caso porventura isso aconteça, a Halex Istar toma as providências necessárias para contingenciar a situação, antes mesmo de concluir a avaliação das causas da ocorrência, muitas vezes promovendo o recolhimento voluntário do produto, em atenção ao princípio da precaução.
6. Foi exatamente o que aconteceu com o lote nº 0000177082 do Produto: a própria Halex Istar promoveu o recolhimento do produto e comunicou o fato à Anvisa em 13.2.2025, que, quase dois meses depois, publicou a RE n° 1.317, de 3.4.2025, como parte natural do procedimento administrativo de recolhimento voluntário iniciado pela empresa (As manifestações da Anvisa, como ente público, devem ser publicadas no D.O.U).
7. Resta informar que o fato objeto da notícia diz respeito exclusivamente ao Lote nº 0000177082 (Fab. 05.23, Val. 05.25), mencionado na RE n° 1.317, de 3.4.2025. De passagem, referido lote já foi majoritariamente recolhido do mercado. A ocorrência em questão, além de pontual, não trouxe qualquer risco sanitário e não impactou nem a produção, e menos ainda a qualidade, segurança e eficácia do Produto. Todos os demais lotes atualmente presentes no mercado consumidor encontram-se em perfeitas condições de uso.
8. A notícia, todavia, peca pela imprecisão, ao deixar de destacar que o recolhimento em questão diz respeito apenas a este lote exclusivamente, e causa rebuliço indevido perante os consumidores, quando deixa de informar tal fato. Isso posto, a Halex Istar requer digne-se esse prestigioso jornal de complementar a notícia com esta relevante informação, para bem esclarecer a população.
9. Ressaltamos o comprometimento da Halex Istar com a segurança, qualidade e eficácia de seus produtos, sendo suas ações adotadas sempre visando a saúde e o compromisso com seus consumidores, que são prioridades para a Companhia."
