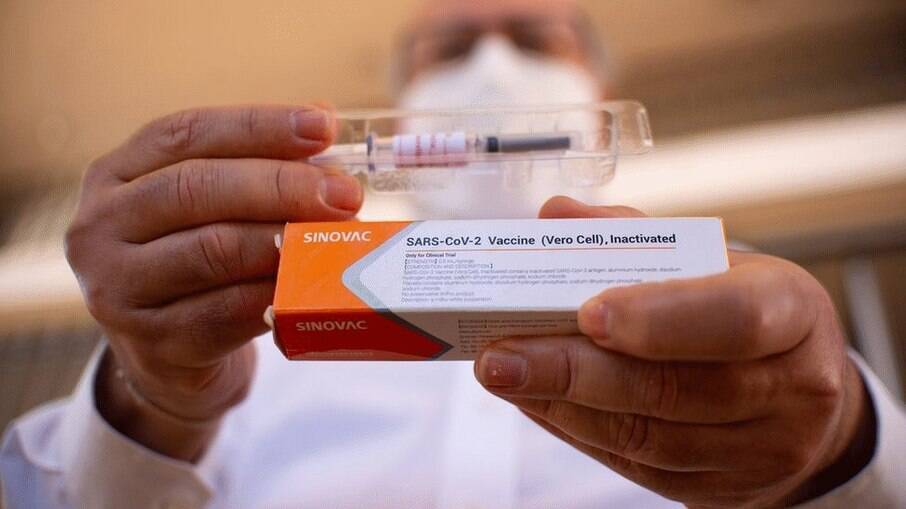
A diretoria da Agência Nacional de Vigilância Sanitária ( Anvisa ) decidiu, em reunião extraordinária nesta quarta-feira (10), prorrogar até 30 de abril o prazo para que o Instituto Butantan apresente os resultados dos estudos de imunogenicidade da vacina Coronavac . Esses estudos, segundo a agência, vão complementar o conhecimento sobre imunidade conferida aos voluntários que receberam a vacina na etapa clínica dos ensaios na fase 3.
A Coronavac teve autorização de uso emergencial aprovado pela Anvisa em janeiro e, junto com a vacina da Astrazeneca , compõe o rol de imunizantes que estão atualmente sendo aplicados no Programa Nacional de Imunização . De acordo com a Anvisa, a chamada imunogenicidade é a capacidade de uma vacina incentivar o organismo a produzir anticorpos contra o agente causador da doença.
Você viu?
"Esse dado é fundamental para que se possa concluir a duração da resposta imunológica nos indivíduos vacinados. A prorrogação do prazo é condicionada a assinatura de termo de aditivo ao Termo de Compromisso já firmado entre Anvisa e Butantan", informou a Anvisa.
Com a prorrogação, o Instituto Butantan pode continuar os estudos necessários para análise do pedido de registro sanitário definitivo pela Anvisa, que avaliará dados de qualidade e dados clínicos adicionais gerados a partir dos testes com as vacinas e a implantação do monitoramento para garantir que as vacinas atendam aos padrões necessários de qualidade, segurança e eficácia.
