
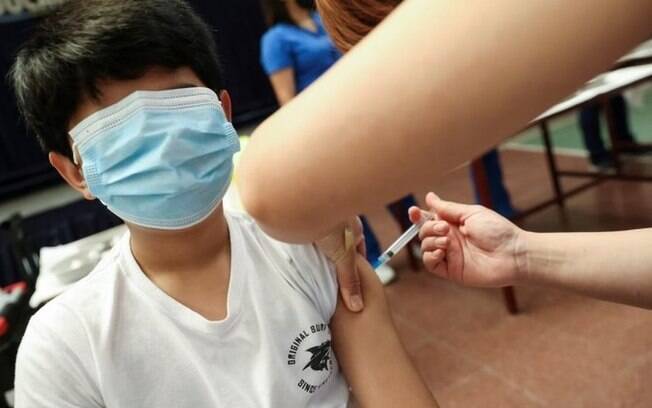
Em reunião realizada nesta quinta-feira (20/1), a Agência Nacional de Vigilância Sanitária (Anvisa) aprovou a CoronaVac para crianças e adolescentes de 6 a 17 anos.
A vacina contra a covid-19, desenvolvida e fabricada pela farmacêutica chinesa Sinovac e pelo Instituto Butantan, em São Paulo, é a segunda a ficar disponível no país para essa faixa etária — a primeira, da Pfizer, já está em uso na campanha de imunização contra a covid-19 dos brasileiros mais jovens.
O pedido do Instituto Butantan era para que a CoronaVac fosse liberada para indivíduos de 3 a 17 anos, a exemplo do que já ocorre em China, Chile, Equador, Camboja e Indonésia, entre outros países.
A Anvisa, porém, decidiu aprovar o uso emergencial a partir dos 6 anos, por considerar que ainda não existem dados suficientes de efetividade do produto em crianças mais jovens (de 3 a 5 anos).
O imunizante que poderá ser utilizado nas crianças é a mesma formulação disponibilizada para adultos, com a aplicação de duas doses num intervalo de 14 a 28 dias entre elas.
Com a aprovação, o Ministério da Saúde pode comprar e começar a utilizar a CoronaVac nas crianças, que foram incluídas agora em janeiro na campanha nacional de vacinação contra a covid-19.
Entenda a seguir os dados que serviram de base para a aprovação da Anvisa e o que já se sabe sobre a efetividade e a segurança desse imunizante na faixa etária pediátrica.
A CoronaVac é efetiva nas crianças?
Durante a reunião, o farmacêutico Gustavo Mendes, gerente-geral de medicamentos e produtos biológicos da Anvisa, fez uma apresentação em que resumiu as evidências científicas sobre o uso da CoronaVac em crianças e adolescentes.
Ele lembrou que o primeiro pedido de liberação desta vacina foi enviado à Anvisa pelo Instituto Butantan ainda em 2021, no mês de julho.
À época, a agência considerou que não tinha informações suficientes para liberar o uso do imunizante no país. 
Uma segunda requisição, que trazia novos estudos, aconteceu mais recentemente, em 15 de dezembro. Desde então, a Anvisa e o Butantan têm feito reuniões constantes, informou Mendes.
Além das pesquisas anteriores, que já tinham determinado a dosagem ideal da CoronaVac para crianças (que segue igual ao utilizado em adultos) e o perfil de segurança do produto, o farmacêutico destacou evidências recentes, que mostram a efetividade da vacina para esse público.
"Nos foi apresentado um estudo de fase três, que é considerado padrão ouro. Trata-se de um estudo global, feito em vários locais, em que foi planejada a inclusão de 14 mil crianças de seis meses a 17 anos em Chile, Malásia, Filipinas, Turquia e África do Sul", relatou Mendes.
Apesar de essa investigação inteira ainda estar em andamento, já foram divulgados dados preliminares sobre a parte do trabalho que está sendo conduzida no Chile.
"Esses dados incluem a população de 6 a 16 anos e comparou a população que recebeu CoronaVac, Pfizer e não vacinados entre junho e dezembro de 2021", continuou o especialista.
Os resultados mostram uma efetividade de aproximadamente 90% da CoronaVac contra os casos mais graves de covid, em que há necessidade de hospitalização.
Mendes então concluiu que as evidências científicas disponíveis sugerem que há benefícios e segurança para utilizar essa vacina nos mais jovens.
Ele sugeriu que, por ora, esse imunizante seja aplicado em crianças de 6 a 17 anos não imunocomprometidas (ou seja, que não apresentam problemas que afetam o sistema imunológico).
Na avaliação do gerente da Anvisa, o uso deste produto na faixa etária dos 3 aos 5 anos ainda carece de mais estudos, que devem ser feitos e divulgados ao longo dos próximos meses.
"A quantidade de dados disponíveis para crianças acima de 6 anos é representativa. Para aqueles abaixo dessa idade, ainda não existe um acompanhamento significativo", justificou.
O parecer de Mendes também levou em conta o ponto de vista e a avaliação de entidades médicas que estão relacionadas ao tema, como a Sociedade Brasileira de Imunizações, a Sociedade Brasileira de Pediatria, a Sociedade Brasileira de Infectologia, a Sociedade Brasileira de Imunologia e a Associação Brasileira de Saúde Coletiva.
Todos esses grupos se mostraram favoráveis à liberação da CoronaVac para crianças de 6 a 17 anos, no esquema de duas doses com um intervalo de 14 a 28 dias entre elas.
Leia Também
A CoronaVac é segura para crianças?
Na sequência, a farmacêutica Helaine Capucho, gerente de farmacovigilância da Anvisa, fez uma avaliação sobre o risco de eventos adversos da CoronaVac entre os mais jovens.
Ela lembrou que mais de 85 milhões de unidades dessa vacina foram utilizadas até agora em adultos na campanha de vacinação contra a covid-19 em curso no país, o que representa 25% do total de doses aplicadas.
"E, quando olhamos em retrospectiva, vemos a redução da taxa de ocupação de UTIs por covid ao longo de 2021. Isso é resultado da vacinação", lembrou.
Leia Também
A gerente revelou que, de acordo com os sistemas de monitoramento da Anvisa, até o dia 15 de janeiro de 2022 foram notificados 38 casos de reações adversas não graves (como dor no local da aplicação, febre e dor de cabeça) a cada 100 mil doses aplicadas de CoronaVac.
Também foram observados 10 reações graves suspeitas a cada 100 mil doses.
Nesse mesmo período, não foi identificado nenhum óbito relacionado a algum efeito colateral após aplicação da CoronaVac.
Vale ressaltar que todos esses dados se referem à população adulta.
Já em crianças e adolescentes, as melhores evidências vêm, mais uma vez, do Chile. Um relatório do Instituto de Saúde Pública deste país calcula que foram aplicadas mais de 640 mil doses da CoronaVac em indivíduos de 6 a 11 anos por lá.
"A taxa de notificações é de 0,11 eventos adversos a cada mil doses. Destes, 94% são considerados 'não graves'", calcula Capucho.
A farmacêutica considerou que o perfil de eventos adversos após a aplicação da CoronaVac em crianças parece ser bem semelhante ao observado em adultos. E mesmo os efeitos colaterais mais graves são considerados raros ou raríssimos. 
Ela também ressaltou que a vigilância e o acompanhamento sobre a segurança das vacinas continua, mesmo após elas receberem o aval da Anvisa — e isso não significa que esses produtos sejam experimentais ou não tenham evidências suficientes.
A CoronaVac foi aprovada para crianças. O que acontece agora?
Com a liberação da Anvisa, a CoronaVac pode agora ser aplicada em crianças brasileiras de 6 a 17 anos.
Para que isso vire realidade, o Ministério da Saúde precisa comprar as doses e distribuí-las para os Estados.
"A Anvisa tem o papel de emitir um parecer para que o Ministério da Saúde, que é quem aplica as vacinas, tenha possibilidades de enfrentar melhor a pandemia de covid-19 e qualquer outro desafio de saúde que se apresente no futuro", discursou o médico Antonio Barra Torres, diretor-presidente da Anvisa.
Numa entrevista recente à CNN Brasil, o ministro da Saúde, Marcelo Queiroga, disse que a CoronaVac será usada em crianças, caso ela fosse aprovada pela Anvisa.
"Sempre queremos que tenha mais insumos, mais vacinas, mais medicamentos disponíveis. Mas é preciso observar os aspectos regulatórios", disse.
"Uma vez havendo a aprovação da Anvisa, como de costume, o ministério vai usar o inteiro teor desta aprovação para que essa ou qualquer outra vacina que seja aprovada para qualquer faixa etária seja disponibilizada para a população brasileira", concluiu.
Em anúncios realizados nos últimos dias, o governo de São Paulo anunciou que tinha reservado 15 milhões de doses da CoronaVac para as crianças.
"A vacinação de crianças é um ponto mais que relevante nesse momento em que observamos pelos gráficos apresentados uma demanda evolutiva de internações de crianças. Isso é um fenômeno de deslocamento epidemiológico, quando se vacina os mais idosos, a pandemia se desloca para os não vacinados", afirmou Dimas Covas, diretor do Instituto Butantan.
"Uma vez aprovada a CoronaVac, o Butantan estará aberto a solicitações. Estamos prontos e otimistas para ajudar o estado de São Paulo e outros estados que assim desejem. Não temos nenhum acordo nesse momento com o Ministério da Saúde, mas estamos abertos a essa possibilidade", concluiu o diretor do instituto.
Até o momento, o governo federal encomendou 20 milhões de doses pediátricas da vacina da Pfizer, que serão entregues aos poucos, até o final do primeiro trimestre de 2021.
A quantidade, porém, é insuficiente para proteger todas as crianças brasileiras: segundo o Instituto Brasileiro de Geografia e Estatística (IBGE), o país tem cerca de 20 milhões de pessoas com 5 a 11 anos.
São necessárias, portanto, 40 milhões de doses para proteger todo esse grupo.
Sabia que a BBC está também no Telegram? Inscreva-se no canal .
Já assistiu aos nossos novos vídeos no YouTube ? Inscreva-se no nosso canal!
